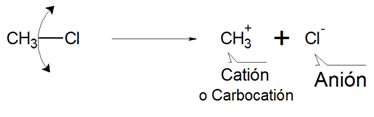
La especie orgánica resultante, CH3+, posee solo seis electrones aparadeados, y en consecuencia adquiere una carga positiva sobre el átomo de carbono, que se denomina ión carbonio o carbocatión.
Los Carbocationes son iones cargados positivamente que contienen un átomo de carbono que cuenta con seis electrones en tres enlaces. Los iones carbonio se representan generalmente como R+.
En segundo lugar es posible que los dos electrones de enlace abandonen el grupo sustituyente (Cl) y sean retenidos por un grupo orgánico (CH3), dando como resultado una especie orgánica con 8 electrones, por lo que el átomo de carbono adquiere una carga negativa y se denomina carbanión o R-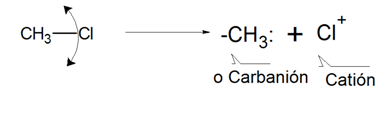
Los Carbocationes son iones cargados positivamente que contienen un átomo de carbono que cuenta con seis electrones en tres enlaces. Los iones carbonio se representan generalmente como R+.
En segundo lugar es posible que los dos electrones de enlace abandonen el grupo sustituyente (Cl) y sean retenidos por un grupo orgánico (CH3), dando como resultado una especie orgánica con 8 electrones, por lo que el átomo de carbono adquiere una carga negativa y se denomina carbanión o R-

ejemplo de rompimiento heterolítico 'carbanión'.
Imagen tomada del blog cienciaslasalleenv.blogspot.com.
Esta imagen fue realizada utilizando el programa ACD/ChemSketch 10.0
Los carbaniones son iones cargados negativamente que contienen un átomo de carbono con tres enlaces y un par de electrones no compartido. Las especies resultantes de una ruptura heterolítica son altamente reactivas, reaccionando rápidamente con otras moléculas. En general, tales especies constituyen sustancias intermedias en las reacciones y se caracterizan por ser de vida muy corta, por lo que no es fácil detectarlas o aislarlas por métodos fisicoquímicos ordinarios.
